L'atome a déjà été imaginé par les grecs, il y 24 siècles, comme la plus petite partie d'un échantillon de matière. chaque atome dépend du type de matière
ATOME vient du grec atomos qui veut dire indivisible.
Depuis le XIXe siécle et l'invention de l'électricité, il a pu être montré que les atomes ne sont pas indivisibles et qu'ils sont tous constitués d'un noyau contenant des PROTONS et de NEUTRONS et d'ELECTRONS en mouvement autour du noyau
Un atome est infiniment petit. Il peut être assimilé à une sphère d'un diamètre d'environ 10-10m ( soit de l'ordre de 0.1 nm).
Le NOYAU au centre de l'atome est environ 100 000 fois plus petit . son diamètre est donc de l'ordre de 10-15 m.
Entre les électrons et le noyau, il n'y a que du vide. On peut donc dire que la matière est essentiellement constituée de vide, on dit qu'elle a un STRUCTURE LACUNAIRE


Le noyau est constitué de deux sortes de particules appelées NUCLEONS:
|
nucléons |
masse |
charge |
|
PROTON |
1.673x10-27 kg |
+e |
|
NEUTRON |
1.675x10-27 kg |
0 |
(avec e =1.6x10-19 C, charge dite élémentaire )
Le NUAGE D'ELECTRONS
|
masse |
charge |
|
| Electron |
9.1x10-31 kg |
-e |
Calcul de la masse de l'atome d'HELIUM:
La masse des électrons peut donc bien être considérée comme négligeable devant celle du noyau.
La masse volumique du noyau d'hélium est de l'ordre de 232 millions de tonnes par cm3 ! Ce serait la masse volumique de la matière habituelle si les noyaux d'atomes étaient jointifs entre eux sans nuages d'électrons. On peut donc dire que la matière habituelle est essentiellement constitué de vide.
conclusion
NOYAU : protons (+) et neutrons(0)
NUAGE ELECTRONIQUE : électrons (-)
Un atome est électriquement neutre:
nombre de p(+) = nombre d'électrons( -)
La masse d'un atome est concentrée dans son noyau:
m(proton) » m(neutron). >>
m(electron).
Donc m(atome) = nombre de nucléon X m(proton)
La matière a une structure lacunaire car elle est essentiellement constituée de vide
Graphe du rayon atomique en fonction du nombre de proton d'un noyau
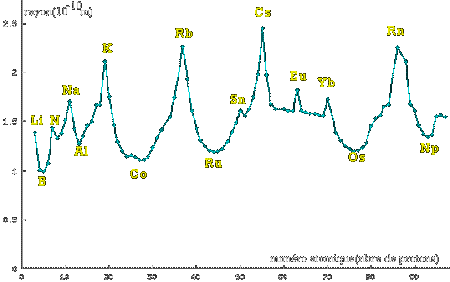
Sur ce graphe sont représentés les rayons d'une centaine d'atomes. On remarque que le rayon d'un atome (donc son volume) ne dépend pas du nombre d'électrons autour du noyau. La valeur moyenne se situe autour de 0.15 nm.